Les exercices
sur 2 exercices complétés
L'éthanol et le méthanol sont deux alcools couramment utilisés. L'éthanol est l'ingrédient principal dans les boissons alcoolisées et il est également utilisé comme désinfectant pour les plaies et les surfaces médicales.
-
Pour réaliser une solution antiseptique, il est nécessaire de prélever une quantité de matière $n = 1,50 \times 10^{-1}$ mol d'éthanol, de formule brute $C_{2}H_{6}O_2$.
- Exprimez, puis calculez la masse $m$ d'éthanol.
- Exprimez, puis calculez le volume $V$ d'éthanol à prélever
- Une bouteille contient un volume $V = 0,750$ L de méthanol.
- Exprimez, puis calculez la masse $m$ de méthanol dans la bouteille.
- En déduire la quantité de matière $n$ correspondante.
Le méthanol, de formule brute $CH_{4}O$, en raison de sa toxicité élevée, est surtout utilisé dans des contextes industriels et techniques comme la fabrication de certaines résines et plastiques ou en tant que composant dans les solutions antigel et les fluides de dégivrage.
Données:
- $\text{M(C)}=12~g.mol^{-1}$, $\text{M(H)}=1~g.mol^{-1}$, $\text{M(O)}=16~g.mol^{-1}$
- $\rho=0,789~g.mL^{-1}$ et $\rho=0,792~g.mL^{-1}$
D'apres Bac Centres Etrangers 2024
Pour titrer le dioxyde de soufre dissous, on utilise une solution de diiode. La solution de diiode étant peu stable, il faut vérifier sa concentration en quantité de matière de $\text{I}_2$ en effectuant un dosage par étalonnage utilisant des mesures d’absorbance.
- La solution disponible étant trop concentrée, on la dilue 10 fois. On note S1 la solution diluée. Décrire le protocole de dilution pour préparer 100,0 mL de solution diluée de diiode en précisant la verrerie utilisée.
- Le spectre d’absorption de la solution diluée S1 de diiode est le suivant :
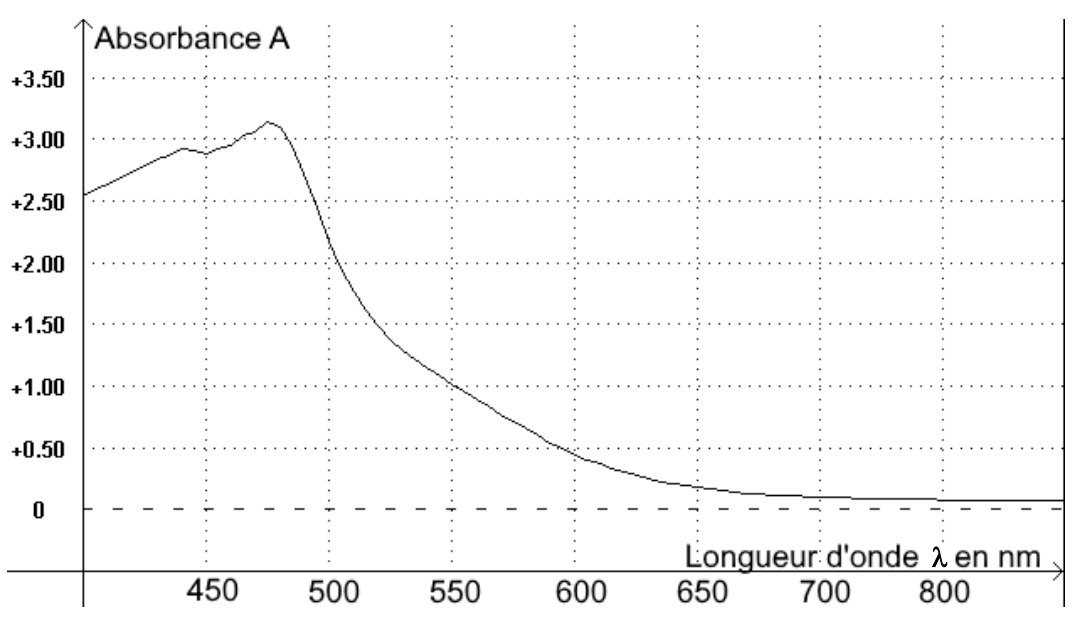
- Déterminer la longueur d’onde pertinente pour laquelle les mesures d’absorbance seront réalisées en exploitant la figure 1. Justifier le choix.
- À partir de S1, on prépare cinq solutions étalons de diiode. On mesure l’absorbance de ces cinq solutions et on trace l’évolution de l’absorbance en fonction de la concentration en diiode.
Montrer que les mesures obtenues pour les solutions étalons de diiode peuvent être modélisées par la loi de Beer-Lambert.
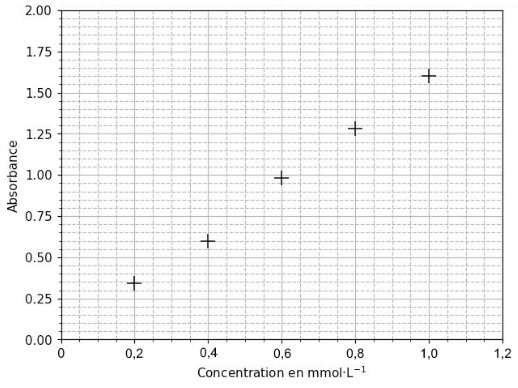
- On mesure la valeur de l’absorbance de la solution titrante de diiode S1 à la longueur d’onde, déterminée à la Q.10 : A1 = 0,80. Déterminer la valeur de la concentration en quantité de matière de diiode de la solution S1.
Contenu Premium
Cette vidéo explicative fait partie de notre contenu premium. Abonnez-vous pour accéder à toutes les méthodes détaillées.
Avec l'abonnement premium :
- Vidéos explicatives détaillées
- Accès à toutes les méthodes
- Exercices corrigés inclus
- Support prioritaire
La mole
Fiche de synthèse
La mole
Contenu Complet Premium
Pour accéder au contenu complet de cette fiche de cours, vous devez vous abonner à notre offre premium.
Avec l'abonnement premium :
- Fiches de cours complètes
- Accès à toutes les méthodes
- Exercices corrigés inclus
- Vidéos explicatives détaillées


